Heb je gehoord van kristallijne versus amorfe typen? De meesten van ons kennen het verschil tussen de twee niet, maar in de biochemische wereld maakt het echt een GROOT verschil voor de stabiliteit.
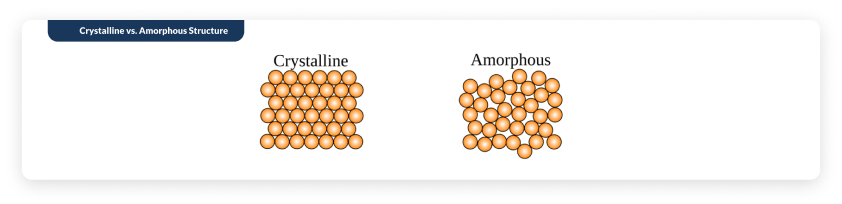
Kristallijne zoutmoleculen worden als extreem stabiel beschouwdHet is bekend dat amorfe zoutmoleculen veel minder stabiel zijn vanwege de hogere blootstelling aan zuurstof. Bekijk de onderstaande afbeelding met een weergave van de structuurverschillen. Het maakt het gemakkelijk in te zien waarom het kristallijne molecuul stabieler zou zijn dan het amorfe (in de gaten zit zuurstof - en dus meer oxidatie en destabilisatie).
Met de unieke C-kristalstructuur,Magnafolaatkan zuurstof goed isoleren, waardoor het bij kamertemperatuur 3 jaar stabiel kan zijn. Eigenlijk grote stabiliteit voor magnafolaatOokbetekent veel zuiverder omdat het niet gemakkelijker wordt afgebroken en schadelijke onzuiverheden met zich meebrengt.

 Español
Español Português
Português  русский
русский  Français
Français  日本語
日本語  Deutsch
Deutsch  tiếng Việt
tiếng Việt  Italiano
Italiano  Nederlands
Nederlands  ภาษาไทย
ภาษาไทย  Polski
Polski  한국어
한국어  Svenska
Svenska  magyar
magyar  Malay
Malay  বাংলা ভাষার
বাংলা ভাষার  Dansk
Dansk  Suomi
Suomi  हिन्दी
हिन्दी  Pilipino
Pilipino  Türkçe
Türkçe  Gaeilge
Gaeilge  العربية
العربية  Indonesia
Indonesia  Norsk
Norsk  تمل
تمل  český
český  ελληνικά
ελληνικά  український
український  Javanese
Javanese  فارسی
فارسی  தமிழ்
தமிழ்  తెలుగు
తెలుగు  नेपाली
नेपाली  Burmese
Burmese  български
български  ລາວ
ລາວ  Latine
Latine  Қазақша
Қазақша  Euskal
Euskal  Azərbaycan
Azərbaycan  Slovenský jazyk
Slovenský jazyk  Македонски
Македонски  Lietuvos
Lietuvos  Eesti Keel
Eesti Keel  Română
Română  Slovenski
Slovenski  मराठी
मराठी  Srpski језик
Srpski језик 








 Online Service
Online Service